細胞融合性タンパク質FASTによる新規ウイルス複製メカニズムの解明(小林研がPlos Pathogens誌に発表)
コウモリ由来高病原性レオウイルス(pteropine orthoreovirus: PRV)は、ヒト呼吸器疾患の原因ウイルスの一つとして知られています。PRVは、細胞融合活性を持つFAST(fusion associated small transmembrane protein)タンパク質をコードしており、感染細胞に強力な細胞融合を引き起こします。FASTタンパク質はレオウイルス科fusogenicレオウイルスグループのみがコードしており、ノンエンベロープウイルス(*1)に認められる唯一の細胞融合性ウイルスタンパク質として知られています。しかし、これまでウイルス複製サイクルにおけるFASTタンパク質の機能については全く分かっておりませんでした。
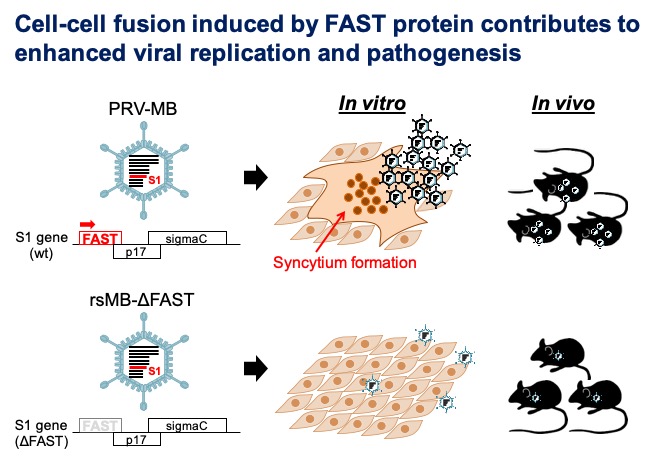
私達はFASTタンパク質の機能を調べるため、PRV Miyazaki-Bali/2007(MB)株の遺伝子操作系を用いて、FASTタンパク質を発現しない遺伝子組換えウイルス(rsMB-ΔFAST)の作製に成功し、FASTタンパク質がウイルス複製に必須では無いことを明らかにしました。rsMB-ΔFASTの増殖能は野生型PRVと比較し、顕著に低下しており、さらに、様々なFASTタンパク質変異ウイルスを作製し、解析した結果、FASTタンパク質による細胞融合活性がPRVの増殖促進に重要な役割を担っていることを明らかにしました。また、FASTタンパク質はFASTタンパク質を持たない分節型2本鎖RNAウイルスの複製を促進することも見出し、これまで不明であったFASTタンパク質のin vitroにおける機能を明らかにしました。
次いで、in vivoにおけるFASTタンパク質の機能について理解するため、動物モデルを用いて解析を行いました。その結果、野生型PRVはマウスに対して致死的な感染を引き起こしますが、rsMB-ΔFAST感染マウスは全く病原性を示さず、FASTタンパク質がPRVの高病原性に関与する主要因子であることが明らかとなりました。さらに、rsMB-ΔFAST感染マウスに野生型PRVを攻撃接種したところ、感染防御効果が認められ、ワクチン候補株として、rsMB-ΔFASTの有用性が示されました。FASTタンパク質変異ウイルスを用いたワクチン開発戦略は、他の病原性fusogenicレオウイルス(トリレオウイルスなど)に対しても応用可能であり、今後の研究の進展が期待されます。
*1 インフルエンザウイルスやHIVを含むエンベロープウイルス(enveloped virus)はウイルス粒子が感染細胞由来の脂質二重膜(エンベロープ)に覆われている。一方、レオウイルスを含むノンエンベロープウイルス(non-enveloped virus)のウイルス粒子はウイルスタンパク質のみで構成される。
本研究成果は、2019年4月25日に科学誌「PLOS Pathogens」(オンライン)に掲載されました。
Cell–cell fusion induced by reovirus FAST proteins enhances replication and pathogenicity of non-enveloped dsRNA viruses
Yuta Kanai, Takahiro Kawagishi, Yusuke Sakai, Ryotaro Nouda, Masayuki Shimojima, Masayuki Saijo, Yoshiharu Matsuura and Takeshi Kobayashi*(*責任著者)