木下研の研究成果がJ Cell Biol誌に掲載されました
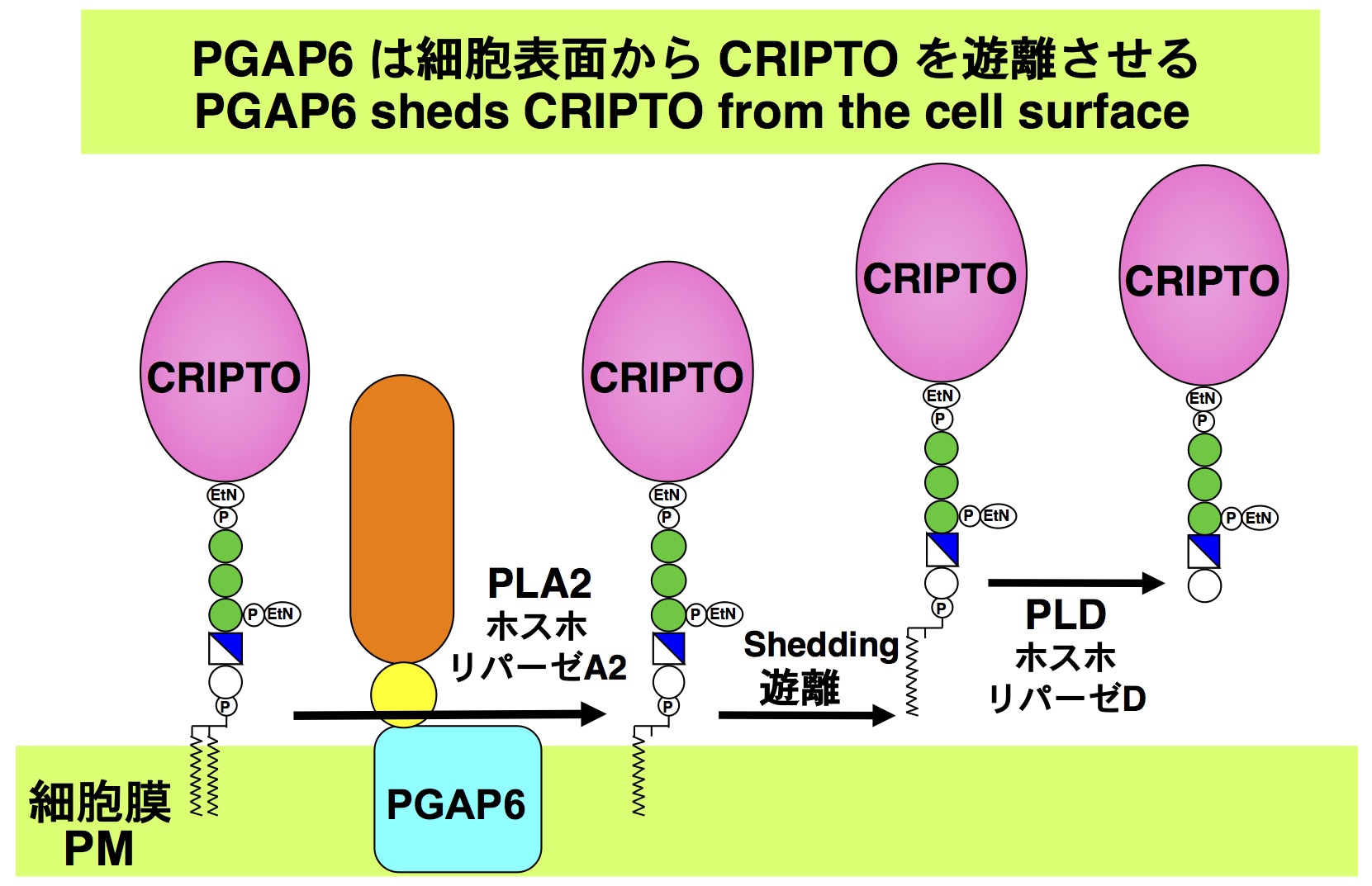
ヒトやマウスなどの哺乳動物では、150種以上の細胞表面タンパク質が、グリコシルホスファチジルイノシトール (GPI) と呼ばれる糖脂質によって細胞膜にアンカーされるGPIアンカー型タンパク質 (GPI-AP、※1) です。GPI-APの特徴の一つは、GPI部分が切断されることによってタンパク質が細胞表面から遊離し得ることです。今回我々は、遺伝子機能解析分野(伊川研)、中央実験室との共同研究により、細胞表面に存在する新規のGPI特異的ホスホリパーゼA2(※2)を発見し、PGAP6と名づけました。そして、PGAP6は初期胚の細胞において、GPI-APであるCRIPTO(※3)のGPIアンカーから脂肪酸を除去し、機能を持ったCRIPTOを細胞外へ遊離させることを見出しました。 CRIPTOはNodal(※3)の副受容体として働き、初期発生に重要な役割を果たしています。PGAP6ノックアウトマウスは胎生致死で、CRIPTOノックアウトマウスと同様に、前後軸の形成不全を示しました。この研究結果は、PGAP6によって遊離することがCRIPTOの働きに重要であることを示しており、GPIアンカーの生理的意義の一端を明らかにしました。
(※1)GPIアンカー型タンパク質(GPI-AP)
小胞体で生合成されたGPIアンカーがGPI付加シグナルを持ったタンパク質と結合し、GPI-APが形成される。今回論文を発表した免疫不全疾患研究分野では、GPIアンカーの生合成と修飾経路に関与する25種以上の遺伝子を同定しており、GPI-APの生物学的・医学的意義の解明を目指し研究を進めている。
(※2)ホスホリパーゼA2
グリセロリン脂質を加水分解し、遊離脂肪酸とリゾリン脂質を産生する酵素群の総称。今回同定されたPGAP6は細胞膜表面に存在するホスホリパーゼA2で、GPIアンカーを加水分解してタンパク質を遊離する。
(※3)CRIPTO、Nodal
前後軸、左右軸の形成や、中胚葉形成など胚の初期発生において重要な機能をもつタンパク質。CRIPTOはNodalとともに受容体に結合し、細胞内シグナル伝達を誘導する。