審良研の研究成果がNature誌に掲載されました
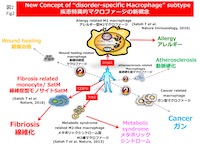
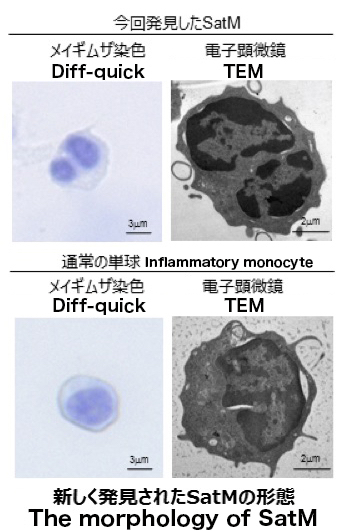
マクロファージはこれまでは体内のごみを食べて処理する役割しかないと考えられていました。研究グループは、線維化期(※1)に患部で増殖する免疫細胞を詳細に解析した結果、数は非常に少ないものの、その病気の発症の原因となる細胞を発見しました。この細胞の形態を調べたところ、通常のマクロファージは核の形態が2核様になっていることが分かりました。さらに、この細胞の遺伝子発現パターン、発現しているタンパクを調べたところ、通常のマクロファージ・モノサイトは殆ど持ち合わせていない顆粒を多く保有していることが分かりました。
研究チームはこの細胞の遺伝情報を用いてバイオインフォマティクスの手法により解析し、SatMの分化にはC/EBPという転写因子(※2)が重要である事を突き止めました。実際免疫細胞でのみこの遺伝子がノックアウトされるマウスを作製したところ、SatMが消失していることが明らかになりました。このマウスに線維症をおこす試薬を投与し、MRIをもちいてin vivo イメージングを行って経時的に解析したところ、病気の発症が著しく抑制されました。これらの研究データから、この細胞は今までに報告が無い新しい細胞であったので、その核の特異的な形態からSegregated Nucleus atypical monocyte (SatM)と名前を付けました(上図)。
更に、SatMは通常のマクロファージの分化経路とは異なる前駆体(SMP)から分化することも明らかにしました。この線維症に特化した疾患特異的マクロファージであるSatMの研究から、未だ明らかとなっていない線維症発症の仕組みの一端がわかりました (図2)。
(※1)線維化
繊維状の結合組織が増殖する現象。障害を受けた組織の治癒過程にも見られるが、過剰な蓄積は正常な組織を破壊し機能不全をもたらす。今回のモデルとなった肺線維症や、肝全体の線維化を示す肝硬変をはじめ、心臓や腎臓など様々な臓器で起こり得る病態である。
(※2)転写因子
様々な遺伝子の発言を制御するタンパク質。DNAに直接結合しmRNAの合成を調節する。