老化細胞を選択的に死滅させる薬剤候補を同定(原研がNat Commun誌に発表)
正常な細胞は発がんストレスを感知するとアポトーシスを起こして死滅するか、細胞老化を起こして細胞周期の進行を不可逆的に停止することが知られています。これらの現象は、異常細胞の増殖を防ぐ重要ながん抑制機構として働いていると考えられています。しかし、アポトーシスとは異なり、細胞老化を起こした細胞(以下、「老化細胞」と呼ぶ)は生存可能なため、加齢とともに体内に蓄積することが分かってきました。さらに体内に蓄積した老化細胞は炎症性サイトカインなどの様々な炎症性物質を分泌するSenescence-associated secretory phenotype (SASP)と呼ばれる現象を引き起こすことで慢性炎症を引き起こし、がんを含めた様々な加齢性疾患の発症を促進することがわかってきました。このため、体内に蓄積した老化細胞を選択的に死滅させる薬剤(セノリティクドラッグ)を開発することが出来れば、加齢性疾患の発症を抑え、健康寿命の延伸につながるのではないかと期待されています。
当研究グループは武田薬品工業(株)のオープンイノベーションプラットフォーム(RINGO-T)を利用し、大規模化合物ライブラリーを用いたハイスループットスクリーニングを行い、セノリティクドラッグの候補物質を15個同定しました。そのうち活性が高かった4化合物がBET(Bromodomain and extra-terminal domain)阻害剤であることがわかりました。そこで、最近開発された強力なBET 阻害剤であるARV825(従来のBET阻害剤にE3ユビキチンリガーゼの結合部位を付加することで、BET- family蛋白質を選択的かつ効果的に分解できる化合物)を、これまでに同定されたセノリティクドラッグ候補薬剤と比較してみました。その結果、ARV825がセノリティクドラッグとしての効果が最も高いことがわかりました。また、ARV825の作用機序を解析したところ、BET- family蛋白質の一つであるBRD4の分解促進を介して老化細胞で働く主なDNA二重鎖切断修復機構である非相同末端結合 (non-homologous end-joining: NHEJ)を阻害すると同時にオートファジー関連遺伝子の発現上昇を引き起こすことで老化細胞の細胞死が起こることを明らかにしました(図1参照)。
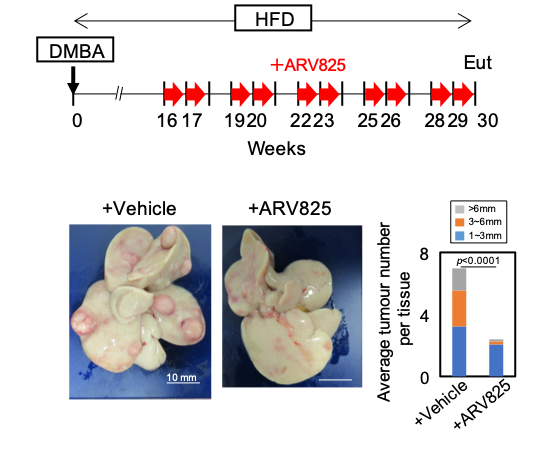
更に、ARV825が生体内でもセノリティクドラッグとして働くかどうかを確認するために、細胞老化を起こした肝星細胞(伊東細胞)によって肝がんの発症が促進されることが知られている肥満マウスにおいてARV825を投与したところ、細胞老化を起こした伊島細胞が減少し、肝がんの発症率も低下することがわかりました(図2参照)。また、ヒトのがん細胞を移植したヌードマウスに抗がん剤 (Doxorubicin)を投与した後にARV825を投与すると、Doxorubicinの投与により発生した老化細胞が減少し、Doxorubicinによる腫瘍抑制効果が増強することがわかりました。最近、抗がん剤や放射線治療で生き残ったがん細胞の一部が細胞老化を起こし、SASPを介してがんの再発や悪性化を引き起こす可能性が報告されており、ARV825のようなセノリティクドラッグは抗がん剤の治療効果の向上にもつながる可能性が期待されます。
これらの発見は、老化細胞の生存維持に関わる分子メカニズムの一端を明らかにすると同時に、そこに関わる分子を標的とすることで有害な老化細胞の蓄積を防ぐことが出来る可能性を示唆しています。今後、さらに研究を続けることで健康寿命の延伸に貢献できるようになることを目指しております。
本研究成果はNature Communicationsにオンライン掲載されました。
【タイトル】A BET family protein degrader provokes senolysis by targeting NHEJ and autophagy in senescent cells
【著者】Masahiro Wakita, Akiko Takahashi, Osamu Sano, Tze Mun Loo, Yoshinori Imai, Megumi Narukawa, Hidehisa Iwata, Tatsuyuki Matsudaira, Shimpei Kawamoto, Naoko Ohtani, Tamotsu Yoshimori, & Eiji Hara