次世代ラッサウイルス弱毒生ワクチン候補株を開発(岩﨑研がmBioに発表)
本研究所の岩崎正治特任准教授(新興ウイルス感染症研究グループ)、米国NIH/NIAID, Integrated Research Facility, Fort DetrickのYingyun Cai リサーチサイエンティスト、米国Scripps ResearchのJuan C. de la Torre教授らの研究グループは、従来とは全く異なる方法でラッサウイルス弱毒生ワクチン候補株を作製し、培養細胞及びモルモット感染実験で安全性、有効性を検証しました。
アレナウイルス科には、致死率の高いウイルス性出血熱を引き起こす病原体が複数含まれます。中でも、ラッサ熱を引き起こすラッサウイルスは人類に対する影響が最も大きく、毎年西アフリカで数十万人に感染し、死者はおよそ5,000人にのぼります。確立された治療法・予防法のないラッサ熱はWHOが指定するBlueprint Priority Diseasesに指定されており、その対策は世界的な課題です。疫学的分析から、ラッサウイルスのコントロールには、一回の接種で長期間の細胞性及び液性免疫を付与できる弱毒生ワクチンが最も有効な手段だと考えられています。これまでに我々は、ラッサウイルスと近縁のリンパ球性脈絡髄膜炎ウイルス(lymphocytic choriomeningitis virus, LCMV)を用いた実験で、1) 非翻訳領域である遺伝子間配列(intergenic region, IGR)が、ウイルスタンパク質発現量を制御すること、また、2) 2分節RNAゲノム(S分節、L分節)のうち、L分節にあるIGR(L-IGR)をS分節のIGR(S-IGR)と置き換えた組換えLCMV [rLCMV(IGR/S-S)]は、ウイルスタンパク質発現バランスが破綻しており、マウス感染実験で高度に弱毒化していることを明らかにしました。本研究では、rLCMV(IGR/S-S)と同様の方法で組換えラッサウイルス[rLASV(IGR/S-S)]を作製(図1)し、弱毒生ワクチンとしての安全性と有効性を培養細胞及びモルモット感染実験で検証しました。その結果、rLASV(IGR/S-S)は以下のような弱毒生ワクチンとして理想的な特徴を有していることが明らかとなりました。
1) 培養細胞では効率よく増殖できる(ワクチン製造コストが抑えられる)
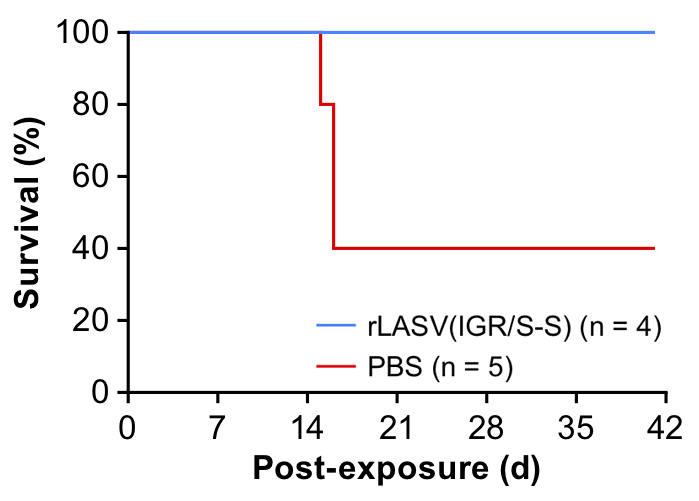
2) モルモット感染実験では、高度に弱毒化しており、かつ致死量の野生型ラッサウイルスによるチャレンジにも100%の個体が生存する防御免疫を付与できる(図2)
3) ウイルスゲノムの安定性が高い(病原性復帰の可能性が低い)
4) IGRは非翻訳領域であるため、rLASV(IGR/S-S)は高病原性親株と同一のアミノ酸配列を維持する
5) 明確な弱毒化メカニズム: IGRの置き換えによるウイルスタンパク質発現バランスの破綻
従来の弱毒生ワクチン作製では、野生型(病原性)ウイルスを様々な種の細胞や動物で繰り返し継代することで、ウイルスゲノムに複数の変異を導入し、ヒトへの病原性を減弱させる方法が取られてきました。しかし、このようなランダムな変異導入による弱毒化では、弱毒化メカニズムの解明がほとんど不可能であり、新たな変異を獲得することによる病原性の復帰を否定できません。本研究の方法は弱毒化のメカニズムが明らかであること、またL分節のIGR全長をS-IGRと置き換えていることから、病原性が復帰する可能性が極めて低いと考えられます。
また、2000年代に入ってからも、ボリビアや南アフリカで新種の出血熱アレナウイルスが出現しており、今後の新型出血熱アレナウイルスの出現も危惧されています。IGRの機能は異なるアレナウイルス種間で共通すると考えられるため、S-IGRをL-IGRと置き換え弱毒生ワクチンを作製する方法は、既知のアレナウイルスに限らず、今後出現し得る新型出血熱アレナウイルスにも応用可能だと期待されます。
本研究成果は、2020年3月24日にアメリカ微生物学会の学術誌『mBio』に掲載されました。
タイトル: A Lassa Virus Live-Attenuated Vaccine Candidate Based on Rearrangement of The Intergenic Region.
著者: Y. Caì#, M. Iwasaki# (#, co-first author), D. Motooka, D. X. Liu, S. Yú, K. Cooper, R. Hart, R. Adams, T. Burdette, E. N. Postnikova, J. Kurtz, M. St. Claire, C. Ye, J. H. Kuhn, L. Martínez-Sobrido, & J. C. de la Torre.