血管内皮幹細胞を発見(高倉研がCell Stem Cellに発表)
血管は全身に張り巡らされ、血液を全身に送り、生命の維持に必須の役割を果たしています。血管は内腔を覆う血管内皮細胞と、その周囲を取り囲む壁細胞から構成されています。血管内皮細胞は血管の構成要素となるだけでなく、血液と組織が酸素や栄養素などの物質交換を行う場として働き、さらには様々な生理活性物質を産生して組織や臓器の機能を維持する働きがあります。
これまで、この血管内皮細胞がどのようにして生体中で維持され、障害された時に修復されるか詳しく分かっていませんでした。細胞の維持・修復は、他の多くの組織では幹細胞が存在し、その役割を担っていることが知られています。従来、骨髄に血管内皮前駆細胞(EPC)と呼ばれる細胞が存在して、血管再生が必要な領域で血管内皮細胞に分化して血管の再構築に貢献していると言われてきました。しかし近年、EPCによる血管への貢献性は一過性であり、長期にわたって血管を構築しうる血管の幹細胞は発見されていませんでした。そこで、我々は血管の再生・維持において中心的な役割を果たす幹細胞が血管壁の中に存在しているのではないかという仮説を立て、血管内皮幹細胞を探索する研究に取り組んできました。
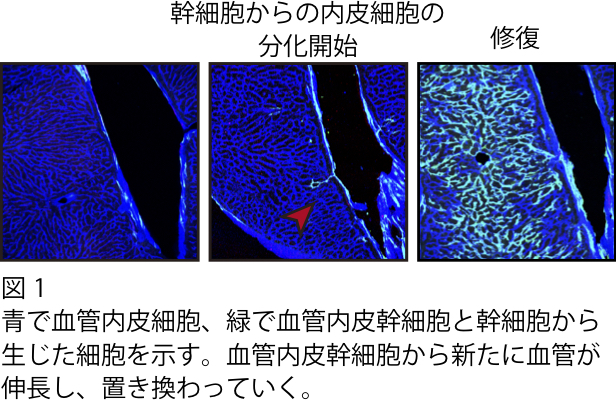
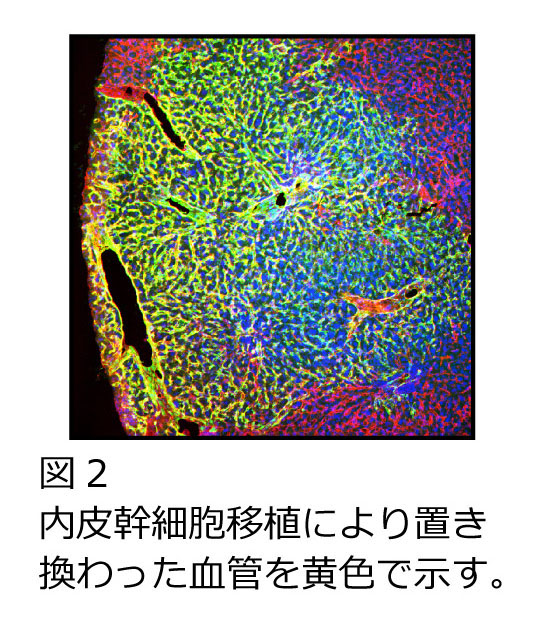
私たちは、これまでに幹細胞の同定法として知られているSide Population(SP)法(原理的には薬剤排出能が高いことで幹細胞を同定する)を用いて、既存の血管の中のごく一部の特殊な血管内皮細胞が大量に血管内皮細胞を産生する能力を有することを報告してきました。そこで、本研究では最初に、その特殊な血管内皮細胞を肝臓の血管から分離して、網羅的遺伝子解析を行うことで、その特殊な内皮細胞に特異的に発現する分子(CD157)を同定しました。CD157陽性の血管内皮細胞は、全身の太い血管の内腔に存在していることが明らかとなりました。またCD157陽性血管内皮細胞は、試験管内で大量に血管内皮細胞をつくり出すことができ、また生体内でも血管が障害された際には多数の血管内皮細胞を作り出して血管を再生させる働きをもつ幹細胞であることが判明しました(図1)。この血管内皮幹細胞を、マウスの血管障害部位に移植すると長期間にわたって血管を再生させることができ、幹細胞を用いた細胞移植法、即ち血管内皮幹細胞移植法をマウスモデルにおいて世界で初めて開発しました。(図2)。
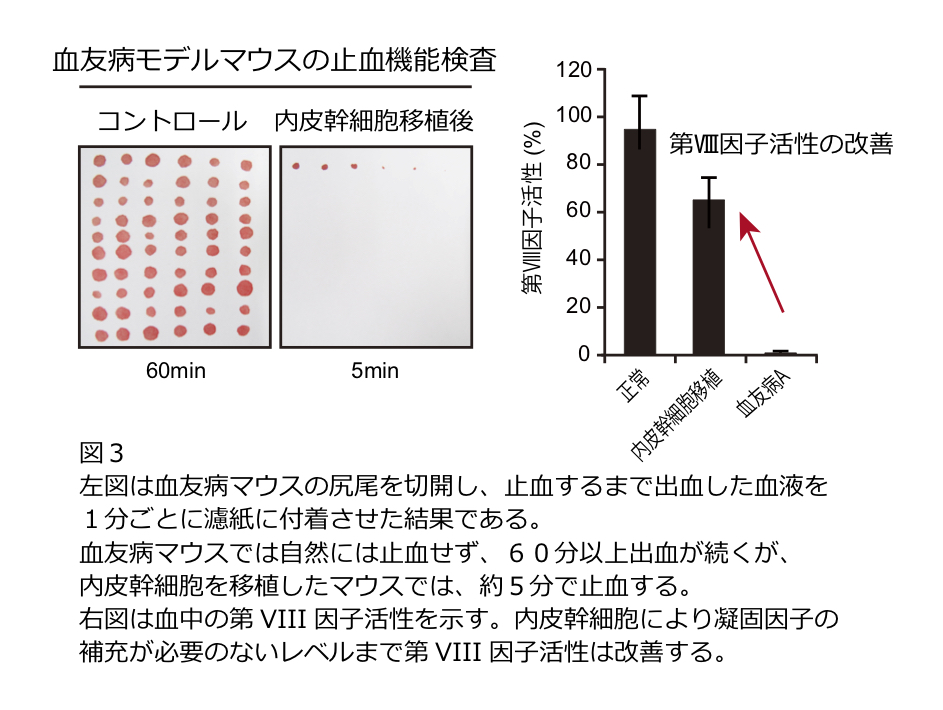
血友病Aでは血液を固める血液凝固因子のうち、肝臓の血管内皮細胞で産生される凝固第Ⅷ因子が低下または欠乏しています。そこで、血管内皮幹細胞移植法を用いて血友病マウスに第Ⅷ因子を産生することができる内皮幹細胞の移植を行うと、肝臓の血管内皮細胞を置き換えることができ、長期間にわたって第Ⅷ因子を作り出すことが可能となり、血友病Aモデルマウスの止血異常を改善することができました(図3)。
本研究により発見された血管内皮幹細胞をより詳細に解析することで、今後血友病や虚血性疾患など血管内皮細胞の機能障害が原因で生じる様々な疾患に対する新たな治療法の開発に大きく貢献することが期待されます。
本研究成果はCell Stem Cell誌オンライン版に2018.2.9に掲載されました。








