感染機構研究部門 感染病態分野/山本研究室
我々は病原体感染からどのように身を守っているのでしょうか。このメカニズムを理解するためには、我々に備わる生体防御機構と、病原体が感染症を引き起こす機構の双方の理解が必要です。感染病態分野では、寄生虫であるトキソプラズマ原虫をモデルとし、宿主と病原体が繰り広げる攻防の分子メカニズムを明らかにすべく研究を行っています。
トキソプラズマ原虫に対する宿主の生体防御機構を探る
トキソプラズマ原虫は胞子虫類に属する寄生虫で、ヒトでは世界人口の3割以上が感染していると言われています。しかし、その効果的な治療法は未だ確立されておらず、胎児やHIV感染患者など免疫抑制状態にある場合は重症化し、最悪の場合、死に至ります。
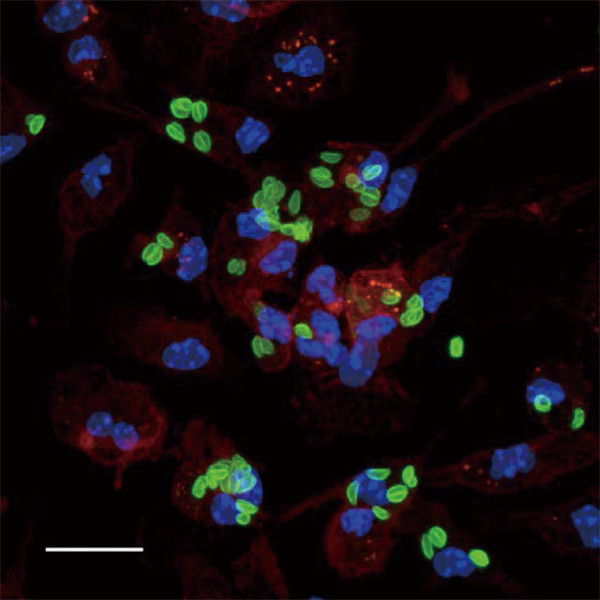
トキソプラズマ原虫は細胞内に侵入すると寄生胞と呼ばれる特殊な構造を形成し感染を成立させます。一方、宿主側はこの寄生胞を破壊し原虫を排除するべく免疫系を活性化させます。この免疫反応にはインターフェロン-γ(IFN-γ)という分泌タンパク質が重要であることがわかっていますが、具体的にIFN-γどのように病原体に対抗するのか、まだ不明の部分が多く残されています。研究室では、IFN-γが誘導する数百種類に及ぶタンパク質に着目し、寄生胞の破壊や原虫の増殖阻止に重要な分子、さらに抗原特異的な免疫反応を誘導するメカニズムを明らかにしてきました。原虫に応答する生体防御機構の全貌を明らかにすべく、トキソプラズマ感染により誘導される免疫応答について現在さらなる解析を進めています。
トキソプラズマ原虫の感染、病態発症の機序解明をめざす
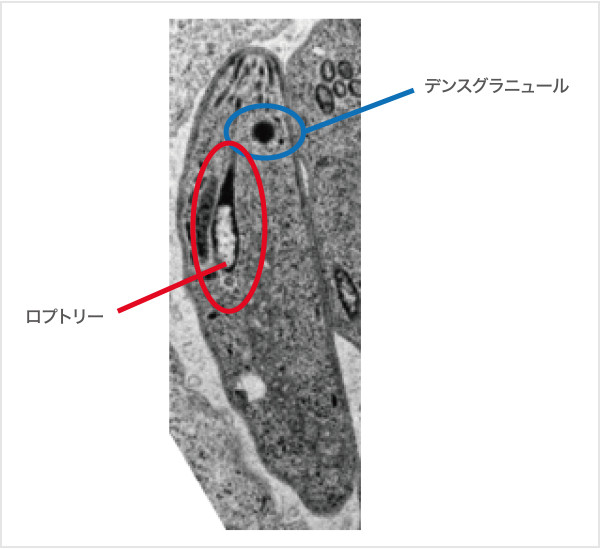
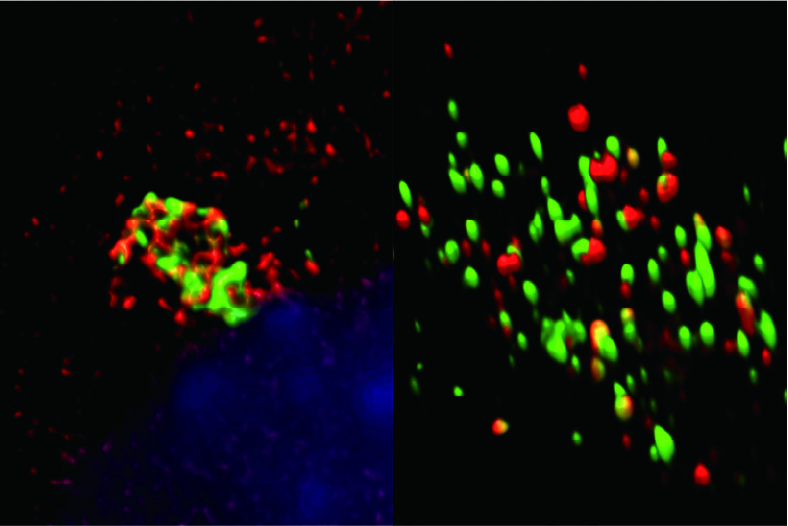
トキソプラズマを始め病原体は、実に巧妙な戦略で我々の体内に入り込み、免疫系を逃れて感染症を引き起こします。それは我々の免疫系や細胞のメカニズムを熟知しているかのようです。つまり、病原体のターゲットを明らかにすれば、我々の生体防御に重要な経路を明らかにすることができるとも考えられます。トキソプラズマ原虫はロプトリーという分泌器官から放出されるROPタンパク質群、デンスグラニュールという細胞内器官から放出されるGRAタンパク群により宿主細胞内で病原性を発揮します。研究室ではROPやGRAタンパク質が宿主のどのような分子を標的としているのか解析を行っています。同定された標的分子の中には、これまで免疫系との関係が知られていなかった分子も発見されており、トキソプラズマの病原性の理解は免疫系のみならず細胞・生体の新たな防御システムの発見や生命現象の理解へと広がることが期待されます。
メンバー
- 教授: 山本 雅裕
- 准教授: 笹井 美和
- 助教: 橘 優汰
- 特任助教: 倉谷 歩見
ホームページ
最近の代表的な論文
- (1) Platelet factor 4-induced TH1-Treg polarization suppresses antitumor immunity. Kuratani A., et al. Science. (2024) 386:eadn8608.
(2) Far-East Asian Toxoplasma isolates share ancestry with North and South/Central American recombinant lineages. Ihara F., et al. Nature Commun. (2024) 15:4278.
(3) Uncovering a novel role of PLCβ4 in selectively mediating TCR signaling in CD8+ but not CD4+ T cells. Sasai M., et al. J Exp Med. (2021) 218:e20201763.
(4) CXCR4 regulates Plasmodium development in mouse and human hepatocytes. Bando H, et al. J Exp Med. (2019) 216:1733-1748.
(5) Essential role for GABARAP autophagy proteins in interferon-inducible GTPase-mediated host defense. Sasai M., et al., Nature Immunol. (2017) 18(8):899-910.
(6) Selective and strain-specific NFAT4 activation by the Toxoplasma gondii polymorphic dense granule protein GRA6. Ma J.S., et al., J Exp Med. (2014) 211:2013-32.
(7) A cluster of interferon-γ-inducible p65 GTPases plays a critical role in host defense against Toxoplasma gondii. Yamamoto M., et al., Immunity (2012) 37:302-13.