細胞社会の秩序はフォースによって守られる(石谷研がScience Advancesに発表)
生体統御分野 石谷太教授、青木佳南特任助教らの研究チームは、九州大学生体防御医学研究所との共同研究により、動物のからだを構成する細胞集団の秩序が細胞間の張力(フォース)によって守られることを明らかにしました。
【研究成果のポイント】
- 動物のからだを構成する細胞が、細胞間張力という物理的な力(フォース)を利用して隣り合う細胞同士で互いに不具合がないか監視し合っていることを発見した。
- 適切に動作できない具合の悪い不良細胞※1が生じると、隣接細胞は細胞間張力の変化を介して不良細胞の出現を感知し、不良細胞に細胞死※2を誘導することがわかった。
- 細胞間張力を介した不良細胞の感知・除去は健康なからだを作るのに必須であり、これが機能しないと細胞の配置があべこべになったり腫瘍が生じたりすることがわかった。
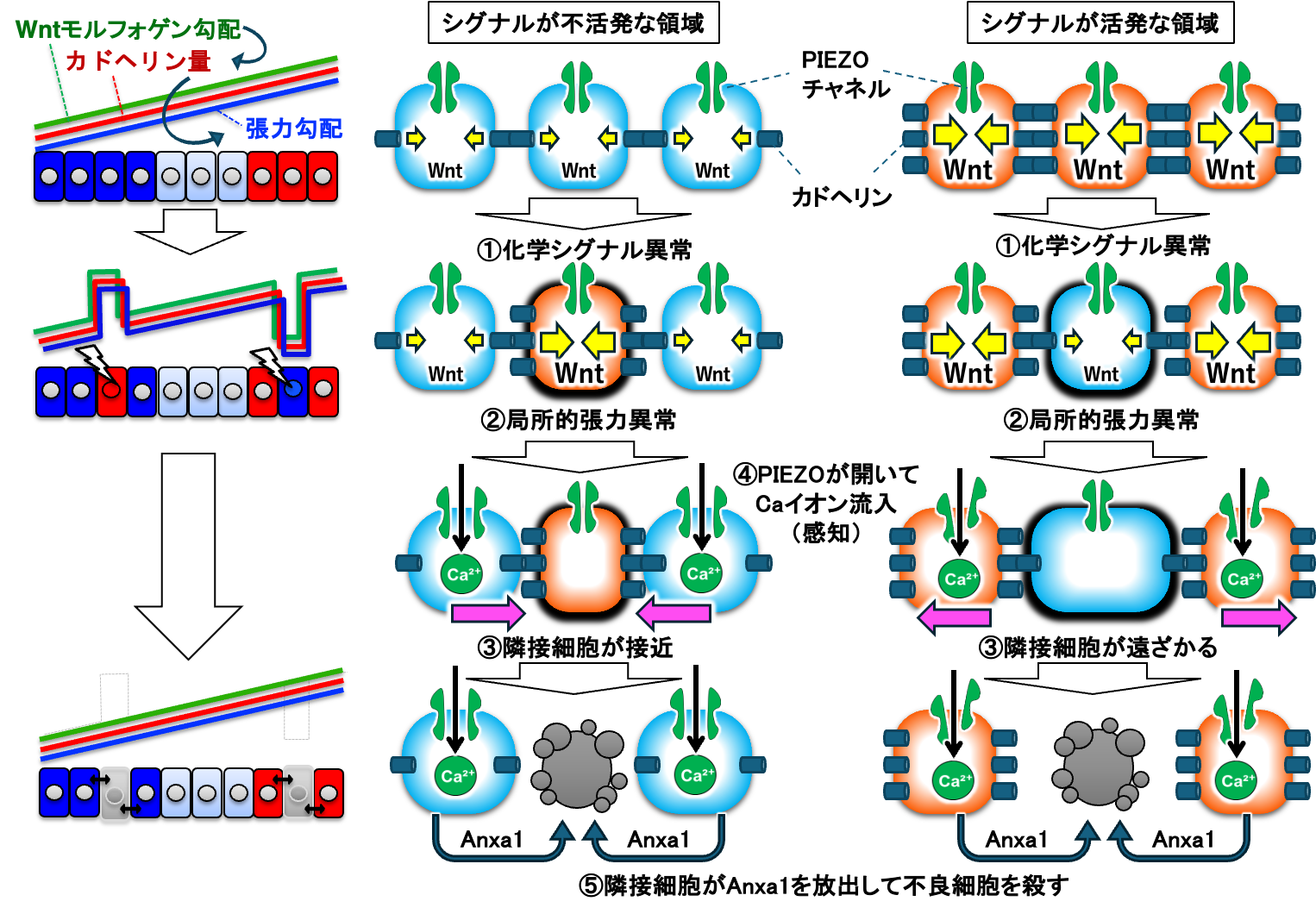
動物のからだづくり(発生)や再生の過程では、細胞が分裂し膨大な数の細胞を生み出しますが、その過程では突発的な異常がある一定の頻度で生じます。これまで、動物組織がこのような異常を回避・克服し、健康性を維持する能力を備えていることは予見されていましたが、この異常回避を担うメカニズムの実体は未知の部分がまだ多く残されています。石谷教授らは以前に、生きた組織の細胞や分子の動態を観察するイメージング解析※3に適したモデル脊椎動物ゼブラフィッシュ※4を用いて、からだを作る細胞集団の中に、発生の進行に必要な化学信号を適切に作動できない不良細胞が頻繁に生じてしまうことと、これら不良細胞が細胞死により除去されることで細胞集団の秩序が回復し、発生が正常に進行できることを明らかにしていました(Akieda et al., Nature Commun 2019※5)。しかしながら、細胞集団がどのようにして不良細胞の出現を感知しているのかは不明でした。今回、研究チームは、引き続きゼブラフィッシュを使った解析を行い、細胞集団が化学信号を細胞間張力(フォース)に変換することによって、隣り合う細胞同士でお互いの化学信号の作動具合を監視しあっており、化学信号を適切に作動できない不良細胞が生じると、隣接細胞は細胞間張力の変化を介して不良細胞の出現を感知し、不良細胞に細胞死を誘導することを発見しました(図1)。また、この細胞間張力を介した不良細胞の感知・除去が、秩序を持った健康な組織・個体を作るのに必須であることも示しました。
この発見は、細胞同士が物理的な力(ひっぱり合う力)を利用してお互いを監視し合うという細胞社会の新たな秩序維持機構の存在を明らかにしたものです。また、同様の機構は、化学信号によって再生・維持される成体の様々な臓器においても起こることが予見され、信号作動が異常な不良細胞を起源として生じるがんなどの疾患に対する防御機構の理解にもつながる知見です。
本研究成果は、米国科学誌「Science Advances」に、2024 年 11 月15日に公開されました。
タイトル:“Mechano-gradients drive morphogen-noise correction to ensure robust patterning”
著者名: Kana Aoki, Taiki Higuchi, Yuki Akieda, Kotone Matsubara, Yasuyuki Ohkawa, Tohru Ishitani
用語説明
※1 不良細胞
機能が破綻した細胞、あるいは、場に不適応で組織機能に負の影響を及ぼしうる細胞。
※2 細胞死
多細胞生物が発生、機関形成する際、生体の恒常性を維持するために細胞が計画的に排除される「アポトーシス」と、組織障害などで細胞が死ぬ「ネクローシス」の2種類がある。本研究における細胞死はアポトーシスを指す。
※3 イメージング解析
生物の体内における細胞動態、細胞内の分子動態を可視化する研究方法。最も多くの情報を得ることができ、生命現象を最も効果的に理解できる方法の一つである。対象とする生物の透明度が高ければ体内深部までイメージングが可能で、かつ対象とする生物が小さければ分子動態、細胞動態、個体の変化を同時に把握できる。このため小さく透明度の高い生物に対して極めて有効である。マウスなど大きな動物で行う場合は、臓器を取り出したりレンズを体内に入れる、あるいは動物を殺して固定し透明化などの処理を施す必要がある。
※4 ゼブラフィッシュ
ヒマラヤ周辺の温帯地域の池の浅瀬や田んぼのそばに棲息するコイ科の淡水魚。胚発生が早く(受精から基本的な体が出来上がるまで24時間程度)、胚が小さく透明なため、イメージング解析に最も適したモデル脊椎動物であると考えられている。また、人と類似した遺伝子、細胞、臓器を有し、かつ、容易に飼育・実験操作できることなどから、「ヒト疾患研究の第3のモデル動物」として米国NIH(国立衛生研究所)に指定されている(第1、第2のモデルはマウスとラット)。本国では同サイズの小型魚類としてメダカが有名であり、近年の研究論文数や研究者人口はゼブラフィッシュの方が圧倒的に多いにも関わらず、よく混同される。メダカが遺伝学解析に適しているのに対してゼブラフィッシュは胚を用いた解析などに適しており、研究用途が異なる。どちらも優れた実験動物である。
※5 Akieda et al., Nature Commun 2019
2019年10月 Nature Communications掲載研究成果
タイトル:“Cell competition corrects noisy Wnt morphogen gradients to achieve robust patterning”
著者名:Yuki Akieda, Shohei Ogamino, Hironobu Furuie, Shizuka Ishitani, Ryutaro Akiyoshi, Jumpei Nogami, Takamasa Masuda, Nobuyuki Shimizu, Yasuyuki Ohkawa, & Tohru Ishitani
https://www.nature.com/articles/s41467-019-12609-4
参考:2019年10月17日プレスリリース
組織・臓器の発生プロセスのエラー回避機構を発見-がんや先天性疾患などの発症機構理解に新たな視点-
https://resou.osaka-u.ac.jp/ja/research/2019/20191017_1