感染機構研究部門 分子細菌学分野/児玉研究室
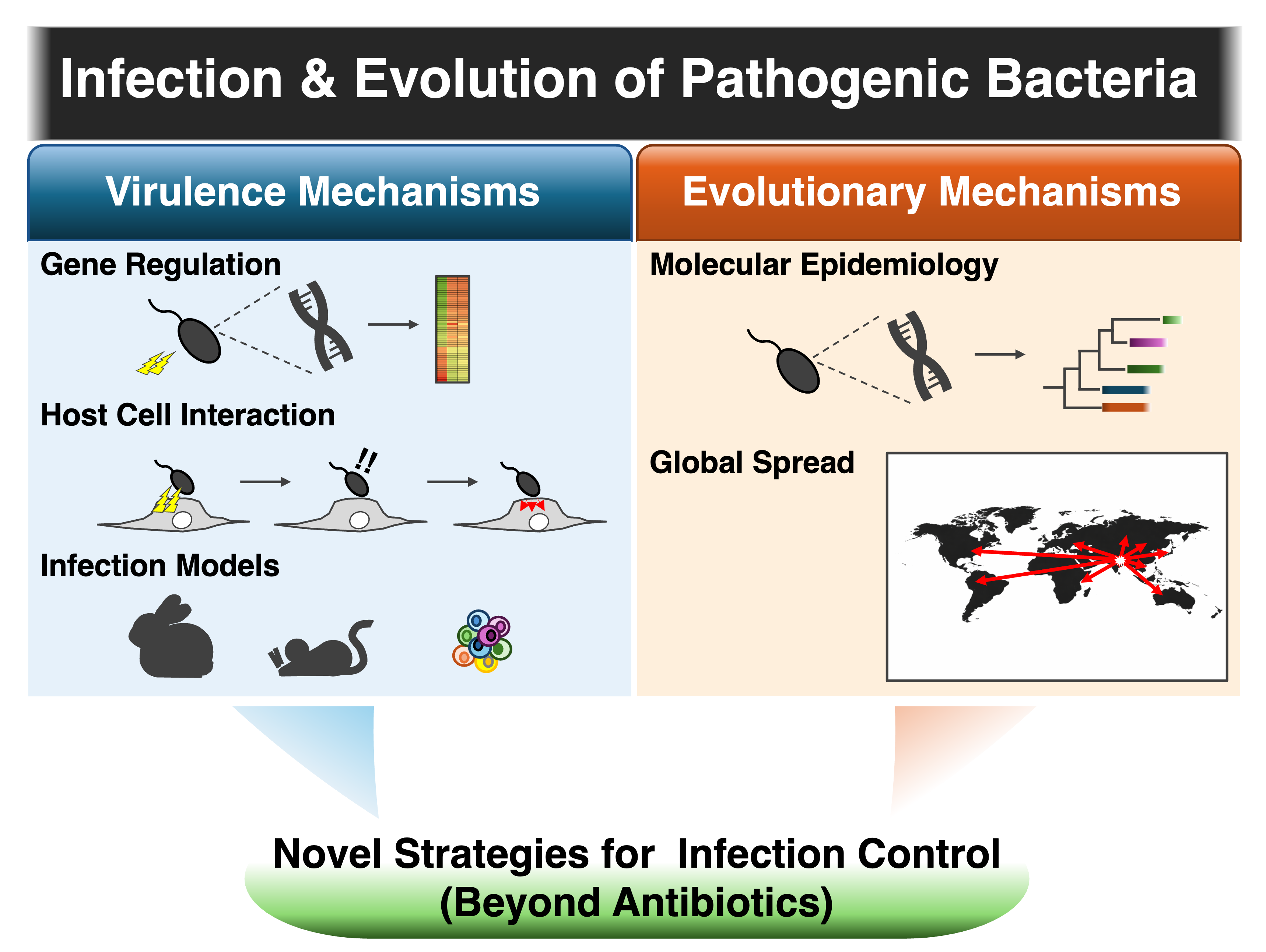
世界的に深刻化する AMR(薬剤耐性)問題 により、抗菌薬のみに依存した感染症制御は限界を迎えつつあります。私たちの研究室では、腸管病原細菌がどのような分子機構によって病原性を発揮するのか、さらにどのような進化過程によって世界的流行株が出現するのかを解明することを目指しています。これらの“仕組み”を理解することで、抗菌薬に依存しない新たな感染症制御戦略につながる概念や手法の創出を目指しています。
腸管病原細菌の病原性発揮の“仕組み”の解明
本研究では、腸管病原細菌がどのような分子機構によって病原性を発揮するのか、その「仕組み」を明らかにすることを目指しています。病原因子の同定からその作用機序、さらに遺伝子発現制御機構に至るまでを統合的に解析し、細菌と宿主の相互作用の分子基盤を解明します。また、新たな感染モデルの確立とその応用を通じて、感染成立の過程を実験的に検証し、細菌と宿主の相互作用を多角的に解析し、感染成立の仕組みの理解を目指しています。
世界的流行を生み出す細菌進化の“仕組み”の解明
国際的な分子疫学研究を通じて、なぜ特定の菌株が世界的流行を引き起こすのか、その進化の「仕組み」を解明することにも取り組んでいます。世界各地で分離された菌株を対象に全ゲノム解析と系統解析を行い、流行株に特異的な遺伝因子や進化的特徴を同定します。さらに、候補遺伝因子の機能を実験的に検証することで、世界的流行株が出現する分子基盤を明らかにすることを目指しています。
メンバー
- 教授:児玉 年央
最近の代表的な論文
(1) Regulatory mechanism for host-cell contact-dependent T3SS gene expression in Vibrio parahaemolyticus. Tandhavanant S. et. al. mSystems. (2025) 10(7):e0025125.
(2) Genomic and pathogenicity analyses to identify the causative agent from multiple serogroups of non-O1, non-O139 Vibrio cholerae in foodborne outbreaks. Morita M, et. al. Microb Genom. (2025) 11(2):001364.
(3) The read-through transcription-mediated autoactivation circuit for virulence regulator expression drives robust type III secretion system 2 expression in Vibrio parahaemolyticus. Anggramukti DS, et. al. PLoS Pathog. (2024) 20(3):e1012094.
(4) Direct RNA Sequencing Unfolds the Complex Transcriptome of Vibrio parahaemolyticus. Al Kadi M, et. al. mSystems. (2021) 6(6):e0099621.
(5) Export of a Vibrio parahaemolyticus toxin by the Sec and type III secretion machineries in tandem. Matsuda S, et. al. Nature Microbiol. (2019) 4(5):781-788.
(6) VopV, an F-actin-binding type III secretion effector, is required for Vibrio parahaemolyticus-induced enterotoxicity. Hiyoshi H, et. al. Cell Host Microbe. (2011) 10(4):401-9.