バイオインフォマティクスセンター 生物情報解析分野 ウイルス情報科学グループ/伊東研究室
COVID-19パンデミックを経て、膨大なウイルスゲノム情報やハイスループット実験データが取得され、ウイルス学はビッグデータ時代に突入しました。本研究室では、これらのビッグデータおよび最先端のAI技術を活用し、ウイルス感染症の制御に貢献するバイオインフォマティクス・AI技術の開発に取り組んでいます。また、新規技術の開発に加え、その技術を用いた大規模データ解析を通じた新たな知見の創出を目指しています。
ウイルスの流行・進化予測するAI技術の開発とワクチン開発への応用
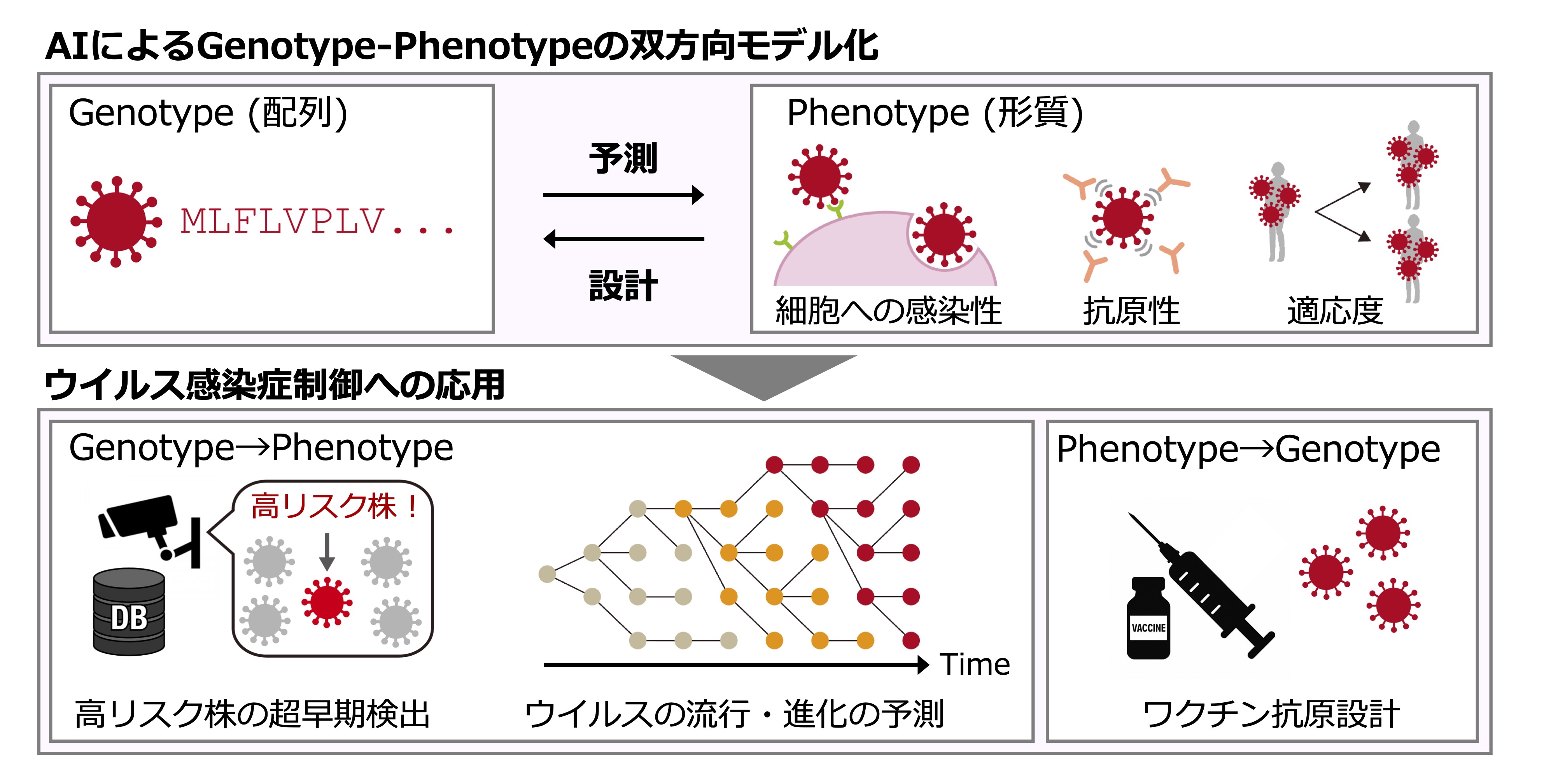
ウイルス感染症の制御が難しい大きな要因の一つは、ウイルスが高い変異率により急速に進化し、その性質を変化させ続ける点にあります。実際、新型コロナウイルスパンデミックでは、免疫逃避能や細胞への感染性を高め、適応度(流行拡大能力)を上昇させた変異株が相次いで出現したことで、流行の制御が困難となりました。本研究室では、タンパク質言語モデルを中心とした最先端のAI技術を活用し、ウイルスのゲノム配列からウイルスの抗原性や細胞への感染性、流行拡大能力(適応度)等の形質を予測する技術の開発を行っています。また形質予測とは逆に、特定の形質(任意の抗原性等)を付与したウイルスタンパク質をデザインする技術の開発を行っています。そしてこれらの技術を、高リスク変異株の超早期検出、ウイルスの流行・進化予測、ワクチン開発・創薬に応用する研究を展開しています(図1)。
ネクストパンデミックウイルス探索のためのAI技術の開発
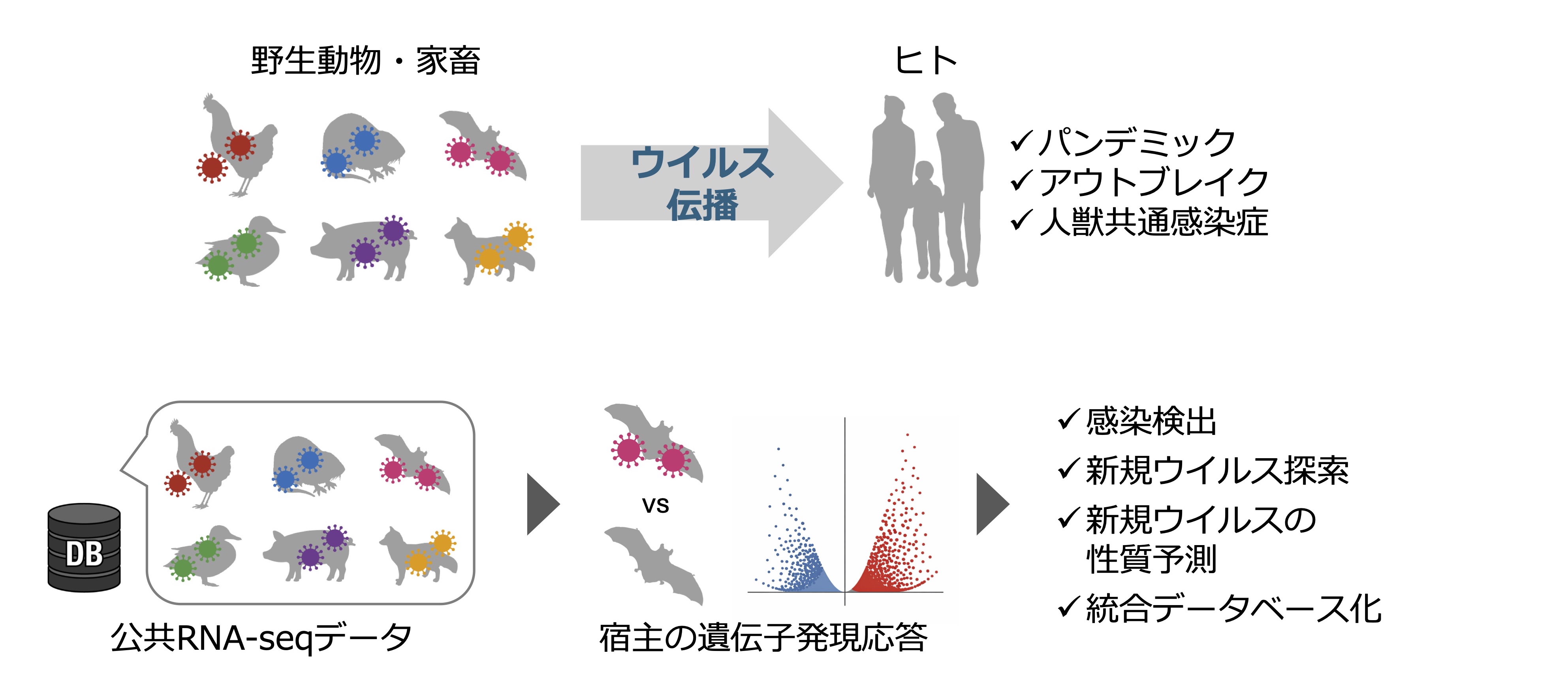
ウイルス感染症の制御を困難にするもう一つの要因は、動物に由来するウイルスがヒトへ異種間伝播し、新たな感染症を突発的に引き起こしうる点にあります。例えば新型コロナウイルスパンデミックは、キクガシラコウモリが保有していたコロナウイルスに由来すると考えられています。将来のパンデミックに備えるためには、野生動物・家畜が保有するウイルスを網羅的に探索し、その性質を明らかにすることが不可欠です。本研究室では、データベースに蓄積した膨大なRNA-Seqデータから、新規ウイルスを網羅的に探索し、その性質やパンデミックリスクを推定する様々なバイオインフォマティクス技術の開発に取り組んでいます。現在は特に、宿主の遺伝子発現応答に基づきウイルス感染を検出、その性質を予測する技術の開発に取り組んでいます(図2)。
メンバー
- 教授: 伊東 潤平
- 特任准教授: 川崎 純菜
- 特任研究員: 菅波麻衣
ホームページ
最近の代表的な論文
(1) Lytras S et al., Inferring context-specific site variation with evotuned protein language models. NAR Genom. Bioinform. In press.
(2) Tsujino S et al., A non-spike nucleocapsid R204P mutation in SARS-CoV-2 Omicron XEC enhances inflammation and pathogenicity. Nat. Commun. (2025) 17:735.
(3) Ito J. et al., Integrative modeling of seasonal influenza evolution via AI-powered antigenic cartography. bioRxiv 2025.08.04.668423.
(4) Ito J, et al., A protein language model for exploring viral fitness landscapes. Nat. Commun. (2025) 16:4236.
(5) Tolentino J. et al., Recombination analysis on the receptor switching event of MERS-CoV and its close relatives: implications for the emergence of MERS-CoV. Virol. J. (2024) 21:84.
(6) Ito J. et al., Convergent evolution of SARS-CoV-2 Omicron subvariants leading to the emergence of BQ.1.1 variant. Nat. Commun. (2023) 14:2671.
(7) Masuda Y et al., Characterization of the evolutionary and virological aspects of mutations in the receptor binding motif of the SARS-CoV-2 spike protein. Frontiers in Virology (2023) Volume 3.
(8) Tamura T et al., Virological characteristics of the SARS-CoV-2 XBB variant derived from recombination of two Omicron subvariants. Nat. Commun. (2023) 14:2800.
(9) Ito J et al., A hominoid-specific endogenous retrovirus may have rewired the gene regulatory network shared between primordial germ cells and naïve pluripotent cells. PLoS Genet. (2022) 18:e1009846.
(10) Yamasoba D et al., Virological characteristics of the SARS-CoV-2 Omicron BA.2 spike. Cell (2022) 185:2103-2115.e19.
(11) Suzuki R. et al., Attenuated fusogenicity and pathogenicity of SARS-CoV-2 Omicron variant. Nature (2022) 603:700-705.
(12) Aso H. et al., Single-cell transcriptome analysis illuminating the characteristics of species-specific innate immune responses against viral infections. Gigascience (2022) 12:giad086
(13) Kumata R. et al., A tissue level atlas of the healthy human virome. BMC. Biol. (2020) 18:55.
(14) Ito J. et al., Endogenous retroviruses drive KRAB zinc-finger protein family expression for tumor suppression. Sci. Adv. (2020) 6(43):eabc3020
(15) Ito J. et al., Retroviruses drive the rapid evolution of mammalian APOBEC3 genes. Proc. Natl. Acad. Sci. U S A (2020) 117:610-618.