BIKEN次世代ワクチン協働研究所 ワクチン創成グループ/吉岡研究室
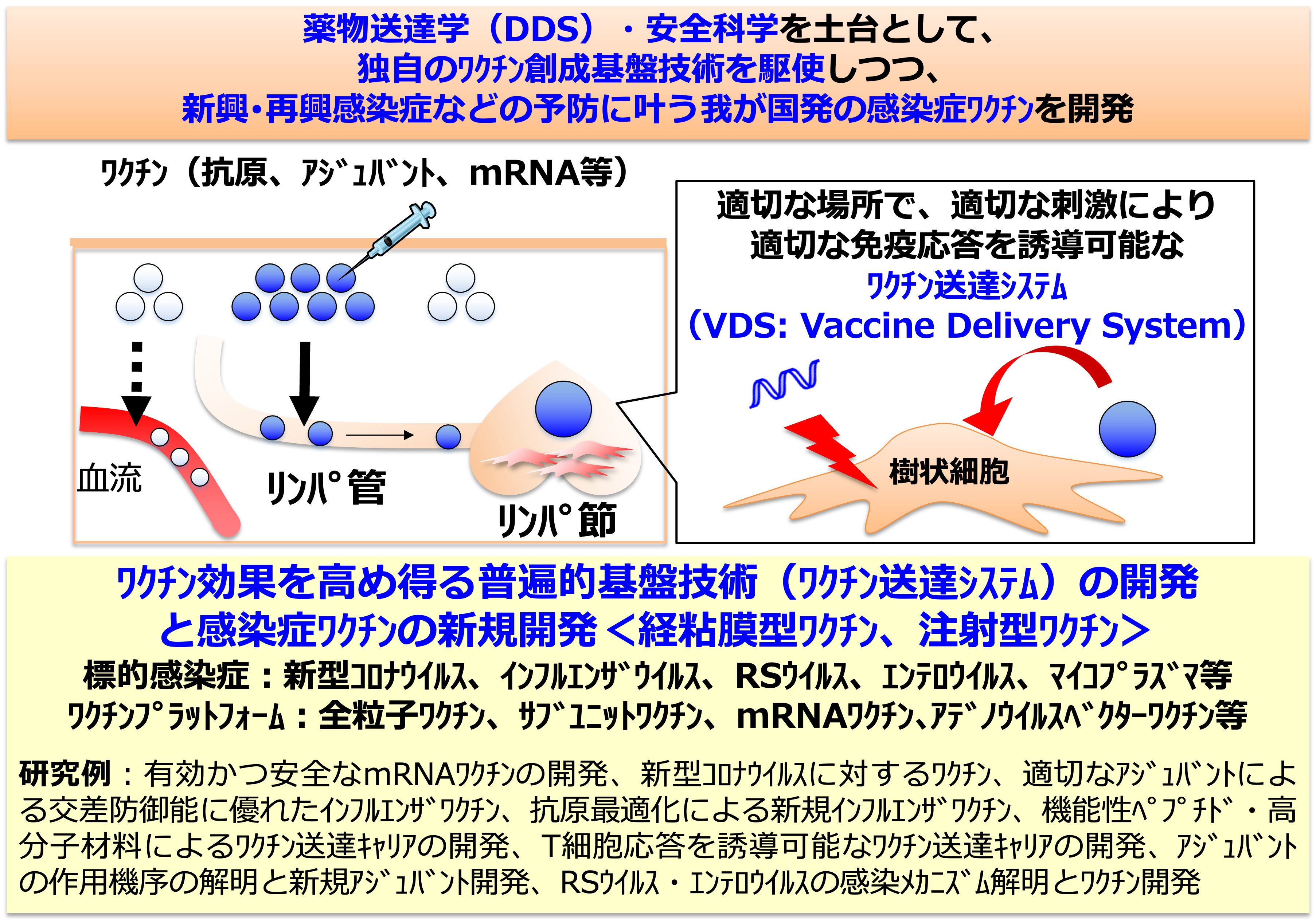
昨今の新型コロナウイルスや新型インフルエンザウイルスの猛威などからも明らかなように、病原性ウイルス・細菌による感染症は未だヒトの健康維持における圧倒的脅威となっている。その点、最強で最善の予防手段であるワクチンの開発が、感染症の克服に向けての鍵となっているものの、ワクチンの存在しない感染症や、効果が不十分なワクチンも多数存在している。例えば2022年、季節性及び動物由来インフルエンザやRSウイルス感染症、エンテロウイルス感染症などが重点感染症に指定され、有効かつ安全なワクチンの開発が待望されている。本観点で我々は、薬物送達学や安全科学を基盤とした薬学的観点から、強力な「ワクチン効果」は当たり前で、老若男女が安全・安心に接種できるワクチン開発を目指している。特に、一般財団法人阪大微生物病研究会との強固な連携のもと、1)サブユニットワクチン、不活化全粒子ワクチン、mRNAワクチン、アデノウイルスベクターワクチンなどのモダリティーやアジュバントについて、薬物送達学を駆使しつつ有効性・安全性の向上を図ると共に、2)新型コロナウイルス、RSウイルス、エンテロウイルス、インフルエンザウイルス、肺炎球菌を含めた様々な感染症に対するワクチン開発を進めるなど、「ワクチン学」研究を推進している。
メンバー
- 特任教授: 吉岡 靖雄(兼)
- 特任講師: 平井 敏郎(兼)
- 特任研究員: 伊藤泰紀(兼)
ホームページ
最近の代表的な論文
(1) Inflammatory mediators of mRNA vaccine-induced adverse reactions in mice. Honda K. et. al. Mol Ther. (2026)S1525-0016(26)00023-7.
(2) mRNA vaccine expressing enterovirus D68 virus-like particles induces potent neutralizing antibodies and protects against infection. Kunishima Y. et. al. Mol Ther Nucleic Acids. (2025)36(4):102731.
(3) Modulating Immunogenicity and Reactogenicity in mRNA-Lipid Nanoparticle Vaccines through Lipid Component Optimization. Kawaguchi Y. et. al. ACS Nano. (2025)19(30):27977-28001.
(4) Hypertonic intranasal vaccines gain nasal epithelia access to exert strong immunogenicity. Hashimoto S. et. al. Mucosal Immunol. (2025)S1933-0219(25)00032-7.
(5) Low-inflammatory lipid nanoparticle-based mRNA vaccine elicits protective immunity against H5N1 influenza virus with reduced adverse reactions. Kawai A. et. al. Mol Ther. (2025)33(2):529-547.
(6) Recombinant RSV G protein vaccine induces enhanced respiratory disease via IL-13 and mucin overproduction. Kawahara E. et. al. NPJ Vaccines. (2024)9(1):187.
(7) Lipid Nanoparticle with 1,2-Di-O-octadecenyl-3-trimethylammonium-propane as a Component Lipid Confers Potent Responses of Th1 Cells and Antibody against Vaccine Antigen. Kawai A. et. al. ACS Nano. (2024)18(26):16589-16609.
(8) Intranasal immunization with an RBD-hemagglutinin fusion protein harnesses preexisting immunity to enhance antigen-specific responses. Kawai A. et. al. J Clin Invest. (2023)133(23):e166827.
(9) Upregulation of Robo4 expression by SMAD signaling suppresses vascular permeability and mortality in endotoxemia and COVID-19 models. Morita M. et. al. Proc Natl Acad Sci USA. (2023)120(3):e2213317120.
(10) SARS-CoV-2 disrupts respiratory vascular barriers by suppressing Claudin-5 expression. Hashimoto R. et. al. Sci Adv. (2022)8(38):eabo6783.
(11) Elucidation of the role of nucleolin as a cell surface receptor for nucleic acid-based adjuvants. Kitagawa S. et. al. NPJ Vaccines. (2022)7(1):115.
(12) Efficient antigen delivery by dendritic cell-targeting peptide via nucleolin confers superior vaccine effects in mice. Matsuda T. et. al. iScience. (2022)25(11):105324.
(13) The potential of neuraminidase as an antigen for nasal vaccines to increase cross-protection against influenza viruses. Kawai A. et. al. J Virol. (2021)95(20):e0118021.
(14) Synergistic effect of non-neutralizing antibodies and interferon-γ for cross-protection against influenza. Shibuya M. et. al. iScience. (2021)24(10):103131.
(15) Neutrophil-Mediated Lung Injury Both via TLR2-Dependent Production of IL-1α and IL-12 p40, and TLR2-Independent CARDS Toxin after Mycoplasma pneumoniae Infection in Mice. Tamiya S. et. al. Microbiol Spectr. (2021)9(3):e0158821.
(16) Murine cross-reactive non-neutralizing polyclonal IgG1 antibodies induced by influenza vaccine inhibit the cross-protective effect of IgG2 against heterologous virus in mice. Shibuya M. et. al. J Virol. (2020)94(12):e00323-20.